Prefazione
Prima di tutto desideriamo ringraziare gli utilissimi commenti forniti da coloro che hanno visionato i risultati delle analisi, effettuate nell'ambito di attività di ricerca scientifica, relative ai prodotti Priorix tetra ed Infanrix Hexa. Le criticità esposte sono infatti state utilissime al fine di aggiungere integrazioni tecnico-scientifiche in grado di chiarire il lavoro svolto. Crediamo infatti che solo attraverso una sana comunione di visioni scientifiche si possa giungere a conclusioni sui dati ottenuti che possano essere utili per l'intera comunità scientifica e per le persone che si rivolgono a lei.
1. Stato dell'arte
Gli studi preliminari (screening non soggetti a conferma) di profilo biomolecolare, metabolomico e proteomico, eseguiti sui prodotti Priorix Tetra ed Infanrix Hexa hanno portato ad un quadro di composizione riassumibile nei seguenti punti:
- Presenza di diversi segnali analitici non associabili a composti noti mediante le ricerche sulle banche dati Metlin 1-2 e KEGG 3. È quindi emerso un quadro associato ad una notevole complessità di composizione dei prodotti commerciali.
- Presenza di proteine non dichiarate in bugiardino nel prodotto Priorix Tetra. Queste ultime possono potenzialmente essere associate a residui del processo produttivo
- Non rilevazione degli antigeni dichiarati all'interno del prodotto Infanrix Hexa. La tecnica di analisi consisteva nella digestione enzimatica con tripsina associata a tecniche di spettrometria di massa. 4-5
Detti dati hanno sollevato diversi commenti soprattutto in merito al punto C - La rilevazione delle proteine viene infatti effettuata utilizzando un approccio standard, riconosciuto a livello internazionale da oltre 10 anni 4, di digestione attraverso l'enzima tripsina 4. I peptidi così ottenuti sono separati cromatograficamente ed analizzati mediante spettrometria di massa 4-5. L'osservazione principale è stata inerente al fatto che nei vaccini sono presenti composti adiuvanti a base di alluminio che potrebbero potenzialmente inibire il processo di digestione enzimatica.
I dati acquisiti successivamente hanno consentito di fornire chiarimenti sostanziali soprattutto in merito alla contestazione rilevata al punto c.
2. Nuovi approfondimenti ed analisi
2.1 Approfondimenti relativi all'analisi del prodotto Infanrix Hexa
Prima di procedere con l'illustrazione dei nuovi dati acquisiti inerenti ai vaccini Hexyon e Gardasil 9, è d'obbligo rispondere al quesito inerente al dubbio sollevato in merito all'inibizione dell'attività proteolitica della tripsina causata dalla presenza degli adiuvanti a base di alluminio nel vaccino Infanrix Hexa. A tal proposito deve essere specificato il fatto che all'interno del digerito triptico è sempre presente un controllo di digestione. Infatti la tripsina utilizzata per eseguire la digestione, pur essendo ingegnerizzata allo scopo di prevenire l'autolisi, presenta una piccola percentuale di quest'ultima che in caso di attività enzimatica porta all'ottenimento del frammento avente m/z 842 e la seguente sequenza peptidica: VATVSLPR. Detto frammento è stato effettivamente rilevato all'interno del digerito triptico del prodotto Infanrix Hexa come verificabile dal cromatogramma di estrazione ionica (Figura 1).
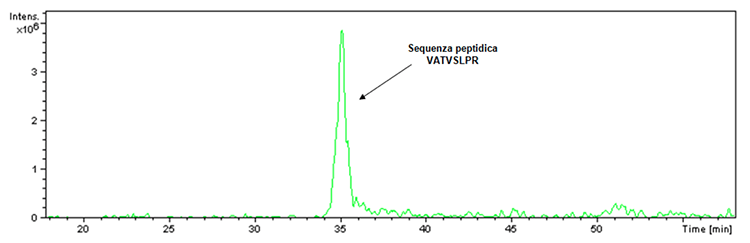
Figura 1: Cromatogramma di estrazione ionica associato allo ione a rapporto m/z 842 rilevato nel campione relativo al lotto del prodotto Infanrix Hexa (lotto n. A21CD072D).
Inoltre, viene eseguito un controllo esterno digerendo emoglobina, allo scopo di verificare ulteriormente la bontà del lotto di tripsina utilizzato. L'emoglobina, analizzata nell'ambito della sezione di analisi in cui era stato monitorato il prodotto, era stata riconosciuta con uno score statistico significativo (loge < -100). Detti dati hanno consentito di confermare il fatto che l'attività dell'enzima era presente.
2.2 Nuove analisi relative ai prodotti Hexyon e Gardasil
L'analisi dei prodotti Hexyon e Gardasil 9 ha portato alla rilevazione di profili molecolari complessi. In detto caso è stata però rilevata la presenza della maggior parte degli antigeni riportati in bugiardino. Essi sono stati rilevati operando mediante digestione triptica ed in presenza di adiuvanti. Questo fatto rafforza ulteriormente l'evidenza che la reazione di digestione triptica non viene inibita in presenza di adiuvanti.
Nel caso dei vaccini Hexyon e Gardasil 9, la complessità di profilo molecolare è stata principalmente attribuita alla presenza di numerose specie, a basso peso molecolare, non identificabili mediante le banche dati di riferimento Metlin 1-2 e KEGG 3.
3. Conclusioni e considerazioni finali
Le analisi effettuate hanno portato a concludere quanto segue:
- Il profilo molecolare dei vaccini analizzati è in generale complesso e in buona parte incognito.
- Sono presenti contaminazioni proteiche, non dichiarate in bugiardino, la cui composizione risulta essere variabile.
- In diversi casi gli antigeni dichiarati in bugiardino non sono stati rilevati. Questo fatto potrebbe essere attribuito a diversi fattori. Tra questi ultimi, possiamo considerare la sensibilità della metodica utilizzata. Tuttavia, ci sentiamo di escludere il fenomeno di inibizione della digestione dovuta dalla presenza di adiuvanti nella formulazione del vaccino. Infatti l'attività enzimatica è confermata principalmente dalla presenza dei frammenti di autolisi triptica, all'interno delle soluzioni dei vaccini digerite (controllo interno).
4. Studi futuri
Saranno effettuati ulteriori studi, nell'ambito delle attività di ricerca e sviluppo volti ad indagare i seguenti aspetti:
- composizione macromolecolare associata ai residui solidi presenti all'interno dei vaccini (Analisi MALDI TOF MS); 5
- valutazione della concentrazione dei metalli presenti all'interno dei prodotti.
- Analisi di secondo livello per confermare la presenza di composti tossici rilevati nella fase di screening. La loro concentrazione sarà quindi rapportata alla tossicità degli stessi in base a quanto dichiarato sulle schede di sicurezza internazionali. Le analisi di secondo livello saranno eseguite in conformità alla direttiva europea EU 2002/657/EC utile per garantire elevati standard di qualità nel settore della spettrometria di massa. 6
in fede
d.ssa Loretta Bolgan
5. Riferimenti Bibliografici
- Autenhahn R, Cho K, Uritboonthai W, Zhu Z, Patti G, Siuzdak G (September 2012). "An accelerated workflow for untargeted metabolomics using the METLIN database". Nature Biotechnology. 30: 826–828. doi:10.1038/nbt.2348. PMC 3666346. PMID 22965049.
- Smith CA, I'Maille G, Want EJ, Qin C, Trauger SA, Brandon TR, Custodio DE, Abagyan R, Siuzdak G (December 2005). "METLIN: a metabolite mass spectral database" (PDF). Ther Drug Monit. 27 (6): 747–51. doi:10.1097/01.ftd.0000179845.53213.39. PMID 16404815.
- Kanehisa M (2013). "Chemical and genomic evolution of enzyme-catalyzed reaction networks". FEBS Lett. 587 (17): 2731–7.
- Cristoni S, Bernardi LR. "Bioinformatics in mass spectrometry data analysis for proteomics studies." Expert Rev Proteomics. 2004 Dec;1(4):469-83.
- Cristoni S, Bernardi LR. "Development of new methodologies for the mass spectrometry study of bioorganic macromolecules." Mass Spectrom Rev. 2003 Nov-Dec;22(6):369-406.
- Cristoni S, Dusi G, Brambilla P, Albini A, Conti M, Brambilla M, Bruno A, Di Gaudio F, Ferlin L, Tazzari V, Mengozzi S, Barera S, Sialer C, Trenti T, Cantu M, Rossi Bernardi L, Noonan DM. " SANIST: optimization of a technology for compound identification based on the European Union directive with applications in forensic, pharmaceutical and food analyses." J. Mass Spectrom. 2017 Jan;52(1):16-21. doi: 10.1002/jms.3895.
Download: CORVELVA-Relazione-Tecnica-Finale.pdf



