Cari amici,
Questo report lo iniziamo in maniera diversa, più emotiva essendo l’ultimo del 2019 ed essendo giunti alla fine di quanto programmato per quest’anno. Si tratta di un documento di riepilogo dei lavori svolti contenente esclusivamente le conferme dei dati che inizialmente erano probabili e che ora sono divenute certe.
Abbiamo terminato i fondi a nostra disposizione per questo progetto e siamo comunque soddisfatti perché avere i conti vuoti in questo periodo di lotta, significa che si sono usate tutte le energie per la battaglia, senza risparmiarci.
Come successo sin dal 2017 ci auto-finanzieremo grazie a quote associative e donazioni di noi genitori e procederemo nel 2020 con tutta una serie di indagini che dovrebbero portare la questione ad un livello superiore ma, nel frattempo, dedicheremo i prossimi mesi ad informare e interagire con le associazioni estere per procedere con la denuncia a livello internazionale. Di lavoro ne abbiamo tantissimo, onestamente sono più le idee che le energie e le possibilità economiche a disposizione.
Insieme abbiamo intrapreso un percorso che è durato parecchio, e oggi siamo riusciti a far conoscere al mondo intero i risultati che questo progetto ha prodotto. La determinazione di noi genitori e cittadini italiani è oggi d’esempio per tante altre nazioni che purtroppo si apprestano a combattere le medesime battaglie in difesa di diritti fondamentali dell’uomo.
Sì, è verissimo, le istituzioni appaiono sorde e non si è mossa ancora una virgola, almeno non in maniera evidente e, cosa più angosciante, i nostri figli sono esclusi dalle scuole, ma guardiamoci attorno: il sistema mondiale gravita attorno al dogma vaccinale supportato da una “comunità scientifica” che, solo in Italia, ha ricevuto più di mezzo miliardo di euro in pochi anni. 1 È una vera e propria pioggia di denaro che ha mosso una schiera di pseudo-scienziati, prezzolati medici e ignavi politici, pronti a tutelare gli interessi di quegli organismi che il Prof. Randy Schekman, Premio Nobel per la medicina nel 2013, ha definito “casta”. 2
“La scienza è a rischio: non è più affidabile perché in mano a una casta chiusa e tutt’altro che indipendente” e questo è oramai evidente anche al più scettico degli spettatori - se in buona fede. Insegue interessi che non sono quelli che accompagnano il metodo scientifico, almeno non come dovrebbe essere; produce studi che per essere pubblicati devono rispettare alcuni dogmi imposti, omettendo alcuni dati che “non convengono” o evidenziandone altri che invece “fanno comodo” e questo lo abbiamo vissuto sulla nostra pelle, pur essendoci solo affacciati a questo mondo.
In questa situazione spregevole ci siamo ritrovati a dover far fronte ad una imposizione di legge per la somministrazione di prodotti farmaceutici, legge che giocoforza va ad arricchire e aumentare il potere di quella casta di cui parla il nobel Schekman.
Dinanzi ad una tale situazione socio-politica ci siamo fatti forza, noi cittadini e genitori consapevoli e determinati, con l’aiuto di altri cittadini come noi abbiamo intrapreso quelle azioni che ci sembravano più efficaci o semplicemente più “abbordabili” in base alle possibilità che avevamo: abbiamo dimostrato che con poche forze, ma con determinazione, si possono produrre grandi risultati.
Siamo partiti con queste poche righe di apertura perché oggi, come ultimo report Corvelva, vi parleremo degli ultimi risultati, che sono conferme arrivate mediante analisi effettuate sia da una prestigiosa università europea che da altri laboratori certificati siti in diverse parti del mondo. I dati sono sempre più certi e ciò che prima era probabile, ora è DIMOSTRATO!
Tra l’altro, abbiamo approfondito una serie di composti tossici e/o cancerogeni come le nitrosodimetilamina NDMA e cianidrine e i risultati sono stati veramente preoccupanti. Di questo ne parleremo obbligatoriamente con pubblicazioni peer review alla mano per non compromettere le pubblicazioni stesse.
Come spiegato, anche questi approfondimenti, come quelli del sequenziamento del DNA fetale, sono oggetto della prossima pubblicazione in peer review, pertanto vi stiamo comunicando veramente una minima parte di ciò che verrà pubblicato, ma così chiede la scienza, che il dato sia inedito. Riportando più dettagli, metteremo il lavoro svolto. Resta comunque il fatto che gli enti di controllo hanno ricevuto tutto, in originale!
Procederemo con l’informazione e combatteremo affinché i risultati, sconvolgenti, vengano considerati per quello che sono, puri dati analitici privi di preconcetti o ideologie. Quei prodotti da noi analizzati sono da ritirare in massa e c’è da porsi un grande interrogativo sugli interessi che gravitano attorno a tutti coloro che si sono posti contro le nostre analisi e/o a favore del dogma vaccinale.
Insieme possiamo tentare di fermare tutta questa follia.
Sintesi dei risultati ottenuti e confermati per ogni vaccino
Per effettuare questa indagine si è scelto di utilizzare un cut-off tra i nanogrammi e i microgrammi, quindi al di sopra del limite residuale per composti non noti e non riportati nella scheda tecnica.
Va sottolineato che la quantità cumulativa di questi contaminanti è al di sopra dei microgrammi per dose, anche se non è possibile al momento fare una quantificazione esatta, in quanto gran parte dei contaminanti non è nota e non è possibile quindi svolgere lo studio mediante standard analitici di controllo.
Dai risultati degli screening e dei controlli con gli standard risulta che la frazione metabolica presenta composti candidati che si spiegano solo con uno scarso controllo, e di conseguenza con la scarsa qualità, delle materie prime e dei reagenti. In particolare, risultano fuori controllo le contaminazioni crociate con composti chimici con attività farmacologica nota, sebbene sia possibile che il processo di produzione del vaccino ne modifichi la struttura e la conformazione originaria.
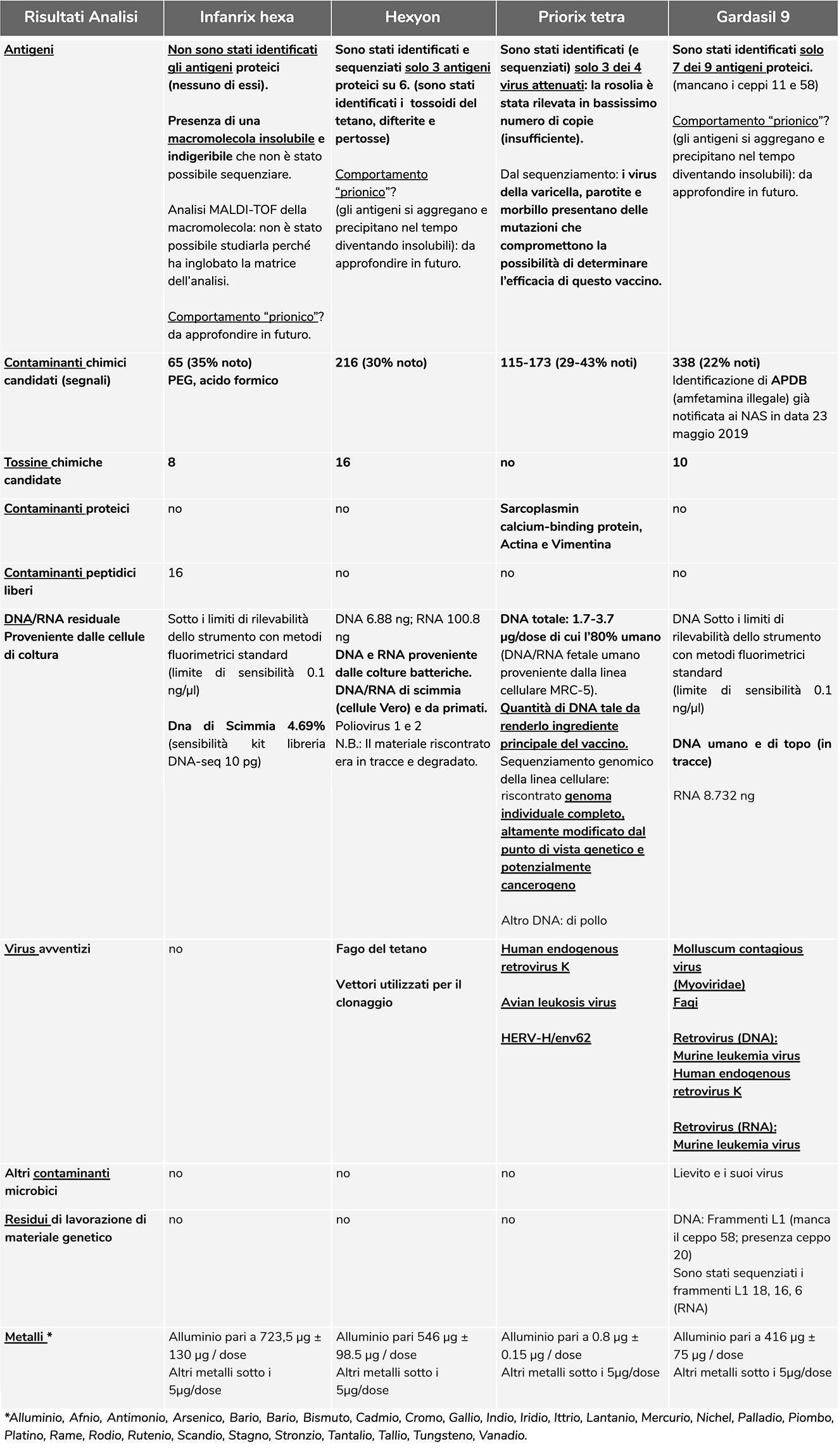
Specifica dei risultati confermati
In fondo a questo sommario riporteremo tutti i link di tutti i report delle analisi eseguite, si faccia sempre riferimento a loro per la comprensione dettagliata dei risultati, poiché qui di seguito parleremo solo delle analisi di conferma mediante screening di secondo livello, standard di controllo e/o interlaboratorio.
Un esempio per meglio comprendere: un service provider certificato ha eseguito alcune analisi su nostra richiesta. È stato loro chiesto di lavorare a target, identificare la presenza o assenza di determinati composti organici o inorganici in determinati vaccini (neppure tutti) o sequenze genetiche. Il risultato pertanto è solo su ciò che abbiamo chiesto di cercare, elemento indispensabile per confermare la validità della metodica da noi utilizzata.
I motivi per non aver utilizzato numerosi standard di controllo e altri vaccini in commercio ha radici economiche e logiche: non siamo un ente di ricerca e stiamo svolgendo approfondimenti, dopo aver segnalato la non conformità agli enti regolatori, che vanno oltre a ciò che a noi dovrebbe competere; a tutti gli effetti ci stiamo impropriamente sostituendo agli enti regolatori stessi in indagini che spetterebbero a loro dopo una segnalazione di questa portata, e lo stiamo facendo perché i nostri dati sono stati definiti incompleti.
Analisi vaccino Hexyon
Metagenomico
La presenza del materiale genetico contaminante è stata confermata con l’analisi interlaboratorio presso un service provider certificato europeo.
Il DNA presente è pari a 6,88 ng totali per dose (tale quantità è riferita al report divulgato. Il dato dell’analisi interlaboratorio è oggetto di peer review e quindi non divulgabile ma conferma l’ordine di grandezza), di cui lo 0,1% proveniente potenzialmente dalle cellule Vero (Cercopithecidae), cioè 688 pg/dose. Abbiamo identificato il Clostridium phage phiCT453A e SV40 assieme ad altri vettori per il clonaggio.
Presenza dei Poliovirus 1 e 2. In questo caso la risposta dell’EMA all’assenza del Poliovirus 3 è stata molto generica, l’assenza non è per loro una non conformità poiché danno per assodato la presenza dell’antigene D, capace di creare immunizzazione. Ovviamente abbiamo cercato questa proteina ma non siamo stati in grado di trovarla, sarebbe un ottimo approfondimento da sviluppare perché attualmente lasciamo su questo punto una risposta incerta.
DNA e RNA dei batteri utilizzati per la produzione degli antigeni di Corynebacterium diphtheriae (Diphtheria), Clostridium tetani (Tetanus), Bordetella pertussis (Pertussis) ed Haemophilus influenzae.
NOTA: il materiale genetico avventizio presente nel vaccino può essere legato all’alluminio adiuvante con possibile potenziamento degli effetti tossici (capacità infiammatoria, autoimmune e tumorale). Ribadiamo che, dai dati confermati interlaboratorio, rimane dubbia anche la sicurezza e l’efficacia di questo vaccino, risultando un prodotto del tutto non conforme per quanto riguarda la qualità.
Analisi vaccino Gardasil 9
Chimico-proteiche
Dopo i precedenti risultati, abbiamo deciso di approfondire l’identificazione, con conferma interlaboratorio, del composto APDB (amfetamina illegale) già notificata ai NAS in data 23 maggio 2019. Due differenti laboratori confermano la presenza di una sostanza appartenente alla classe delle APDB illegali.
Noi, lo ripetiamo, non possiamo acquistare lo standard di controllo essendo l’APDB classificata come stupefacente, 3 non è acquisibile da soggetti non provvisti di apposita autorizzazione, perciò abbiamo fornito tutta la documentazione che conferma la presenza di una sostanza appartenente alla classe delle APDB e la possibile origine della contaminazione (Nota: È riportato nell’assessment report dell’EMA per la registrazione del Gardasil 9 che la L-tirosina viene usata come materia prima per la produzione di questo vaccino e viene estratta da capelli umani provenienti dalla Cina. 4 La produzione principale di questo narcotico proviene dalla Cina e i tossicodipendenti hanno un livello molto alto nei capelli. 5
Metagenomico
La presenza del materiale genetico è stata confermata con l’analisi interlaboratorio presso un service provider certificato europeo e possiamo ripetere i precedenti dati, sono presenti:
- DNA umano e di topo (sotto i limiti di rilevabilità dello strumento)
- Virus avventizi:
- Frammento L1 del virus HPV di DNA a doppia catena;
- Fagi;
- Molluscum contagiosum virus;
- Retrovirus:
- Virus della leucemia murina;
- Retrovirus endogeno umano K.
- Saccharomyces
NOTA: il materiale genetico avventizio presente nel vaccino può essere legato all’alluminio adiuvante con possibile potenziamento degli effetti tossici (capacità infiammatoria, autoimmune e tumorale)
Analisi vaccino Priorix Tetra
Metagenomico
La presenza del materiale genetico è stata confermata con l’analisi interlaboratorio presso un service provider certificato europeo. Le quantità sono riferite ai report divulgati. I dati dell’analisi interlaboratorio sono oggetto di peer review e quindi non divulgabili ma confermano l’ordine di grandezza
DNA - La quantità di DNA totale presente in questo vaccino oscilla da: 1.7 – 3.7 ?g/dose ed è a tutti gli effetti il componente principale del vaccino. Il DNA è di tipo umano circa all’80% (74-88%) e di pollo (0-4%).
Il genoma umano è completo, cioè con geni e sequenze non codificanti, ad alto peso molecolare, di sesso maschile, qualificato come appartenente alla linea fetale MRC-5 cioè la linea cellulare continua derivata da tessuto polmonare di feto abortivo maschile degli anni ’60. Il sequenziamento di questa linea cellulare ha dato prova di come fosse altamente modificato dal punto di vista genetico e potenzialmente cancerogeno. Le analisi di sequenziamento del genoma intero del DNA fetale è stata effettuata presso un service provider (laboratorio) americano.
RNA - Umano 68-87%. Pollo 0-0.2%
Virus attenuati - Sono stati confermati i seguenti virus attenuati lot. A71CB256A:
- Varicella (DNA) 11%;
- Parotite (RNA) 0.008%;
- Morbillo (RNA) 0.004%;
- Rosolia 0.00004%. (114 su 260 milioni di sequenze)
È stata confermata interlaboratorio una presenza irrilevante di rosolia nel vaccino (inferiore ai virus avventizi indicati qui sotto). Ciò mette in serio dubbio l’efficacia del vaccino.
Quasi-specie virali: nel genoma della varicella vaccinale sono state individuate 245 varianti rispetto al genoma di riferimento utilizzato per l’analisi (genoma selvatico del ceppo Dumas). Di queste varianti, 154 sono varianti maggiori mentre le restanti 91 sono varianti quasi-specie. Dal confronto tra le varianti trovate nei due lotti non emerge alcuna differenza. Nel genoma vaccinale della parotite sono state individuate 40 varianti quasi-specie rispetto al genoma di riferimento utilizzato per l’analisi (genoma vaccinale Jeryl-Lynn), Dal confronto tra le varianti trovate nei due lotti emergono 4 differenze. L’EMA non è stata in grado di fornirci le sequenze dei virus vaccinali utilizzati dal produttore per questo vaccino, in quanto coperte da segreto industriale, motivo per cui non sappiamo quanto siano mutati i virus vaccinali rispetto a quanto dichiarato dal produttore
A causa delle coperture basse non è stato possibile rilevare varianti quasi-specie per i genomi di morbillo e rosolia.
Virus avventizi - Abbiamo confermato la presenza di questi virus avventizi:
- Human endogenous retrovirus K;
- Avian leukosis virus;
- HERV-H/env62.
Per tutti i vaccini
Analisi con standard di controllo e interlaboratorio sulle contaminazioni chimiche
Sono stati scelti due composti da analizzare con standard di controllo certificati, sulla base della reperibilità, della consistenza del dato semiquantitativo e per l’impatto per la salute. Questi composti sono stati confermati come similari (cioè con un’identità strutturale del 75-80%: isomeri/isobari) anche mediante l’analisi inter-laboratorio. La struttura di questi composti sarà resa nota con la pubblicazione peer review.
Screening di secondo livello sulle contaminazioni chimiche
L’indagine di screening di secondo livello, come già accennato, si divide in tre analisi:
- screening approfondito della parte sommersa (65% del totale dei segnali) e confronto in banca dati delle sostanze rilevate, compresa la banca dati delle tossine.
- analisi delle perdite neutre: la rilevazione di frammentazioni stabili neutre ci permette di ipotizzare la presenza nel vaccino di molecole che le contengono, di struttura non nota, ma con potenziali effetti tossici se i gruppi funzionali hanno un’attività cancerogena e mutagena (la "Coorte di preoccupazione" creata dall’EMA per i farmaci per uso orale comprende composti aflatossina-simile, N-nitroso- e alchil-azossi, come riportato nella ICH guideline M7(R1). 6
Nuovi composti candidati: sono stati identificati per tutti i vaccini esaminati dei composti potenzialmente tossici (contaminazioni crociate) sulla base del confronto con le banche dati. Sarebbe utile l’approfondimento mediante standard di controllo per confermarne l’identità.
Perdite neutre: Nel nostro caso sono stati esaminati i gruppi cianilici (cioè derivati dall’acido cianidrico utilizzato per la preparazione del vaccino Haemophilus B) e la nitrosodimetilamina, impurezza cancerogena riscontrata in altri farmaci e oggetto di valutazione da parte dell’EMA. 7
Per comprendere il gruppo funzionale delle nitrosodimetilamina, si pensi che è della stessa classe delle contaminazioni riscontrate nei farmaci sartani e ranitidina, balzato alle cronache per il recente massiccio ritiro di farmaci in tutta Europa. 8 Il secondo gruppo funzionale è quello dei cianuri, di cui conosciamo la presenza dichiarata del sodium cyanide come si evince dalle schede tecniche del vaccino Prevenar. 9
Lo screening di secondo livello ha dato quindi risposta positiva per tutti i vaccini. Non è possibile al momento divulgare i risultati nel dettaglio perchè in fase di pubblicazione peer review ma tutti gli enti regolatori sono state messe a conoscenza dei nostri risultati.
La normativa
Si fa presente quanto deve essere effettuato per legge sui farmaci in commercio: 10
Il Programma Annuale di Controllo permette di garantire che i farmaci commercializzati corrispondano esattamente alle specifiche di qualità delle procedure autorizzative. Esso viene stabilito ogni anno dall’AIFA, sentito il parere dell’Istituto Superiore della Sanità, e viene approvato dalla Commissione Tecnico Scientifica (CTS) dell’AIFA. L’Ufficio Qualità dei Prodotti dell’AIFA richiede ai carabinieri del NAS di prelevare, presso le farmacie o i grossisti, campioni dei medicinali previsti nel programma, che vengono inviati all’ISS per l’analisi. Qualora i risultati dell’analisi rilevino delle difformità da quanto autorizzato, l’Ufficio Qualità dei Prodotti dell’AIFA prende i necessari provvedimenti. Le analisi effettuate si basano sulla verifica della rispondenza alle specifiche di qualità autorizzate per ciascun farmaco e riportate nel dossier di registrazione e/o nelle monografie di Farmacopea Europea. (…)
L’Ufficio Qualità dei Prodotti gestisce, altresì, le attività di revoca d’ufficio e di sospensione delle AIC dei medicinali.
L’AIC di un medicinale può essere revocata, con conseguente definitivo ritiro dal commercio quando:
- il medicinale risulta nocivo nelle normali condizioni di impiego;
- il medicinale non possiede l’effetto terapeutico o l’effetto per il quale è stato autorizzato;
- il rapporto rischio/beneficio non è favorevole nelle normali condizioni d’impiego;
- il medicinale non presenta la composizione qualitativa e quantitativa dichiarata;
- il medicinale è stato prodotto in stabilimenti non autorizzati.
L’autorizzazione può essere revocata anche nel caso in cui si riscontri che le informazioni presenti nella domanda di autorizzazione del medicinale non siano corrette o in assenza di controlli sul prodotto finito, sui componenti o sui prodotti intermedi della produzione.
In aggiunta agli interventi adottati a livello nazionale sono contemporaneamente espletate le misure del Sistema di Allerta Rapido, definito in base a procedure condivise a livello europeo, che prevede azioni e notificazioni differenti in relazione alla tipologia di gravità del difetto in accordo con la classificazione delle urgenze.
Nella Figura 2 vengono descritte la classificazione dei difetti e le relative azioni da intraprendere
Si fa notare che i difetti rilevati con le analisi svolte da Corvelva rientrano nella Classe I e II, in quanto i vaccini sono farmaci ad uso iniettivo e le contaminazioni rilevate sono di tipo chimico e di materiale genetico.
Si sottolinea che ad oggi nessun provvedimento è stato intrapreso dalle agenzie regolatorie, nonostante la notifica all’AIFA dei risultati delle analisi preliminari e ai NAS della presenza del composto APDB nel vaccino Gardasil 9, e ciò è in grave violazione del principio di precauzione e della necessità di intervento rapido come previsto dal Sistema di Allerta per la tutela della salute pubblica.
Download: CORVELVA-Sommario-conferme-dati-analisi-interlaboratorio.pdf
Note:
- https://www.corvelva.it/it/approfondimenti/sistema-sanita/case-farmaceutiche/efpia-italia-tutti-i-trasferimenti-di-valore-delle-big-pharma.html
- http://www.medicinapiccoledosi.it/medicina-convenzionale/premio-nobel-la-medicina-randy-schekman-la-scienza-mano-ad-casta/
- http://www.cortedicassazione.it/cassazione-resources/resources/cms/documents/Legge_79_2014.pdf
http://www.rivistagiuridica.aci.it/fileadmin/Documenti/Decreto_25_giugno_M_Salute_02.pdf - https://www.unodc.org/documents/scientific/Trends_and_Patterns_of_ATS_and_NPS_2017.pdf
- Gas Chromatography-Mass Spectrometry (GC-MS) AnalysisJournal of Food and Drug Analysis, Vol. 13, No. 3, 2005, Pages 193-200Gas Chromatography-Mass Spectrometry (GC-MS) Analysis of Amphetamine, Methamphetamine, 3,4-Methylenedioxy- amphetamine and 3,4-Methylenedioxymethamphetamine in Human Hair and Hair SectionsDONG-LIANG LIN1,2*, REA-MING YIN1 AND RAY H. LIU3
- https://www.ema.europa.eu/en/documents/ … /ich-guideline-m7r1-assessment-control-dna-reactive-mutagenic-impurities-pharmaceuticals-limit_en.pdf
- http://www.agenziafarmaco.gov.it/content/comunicazione-ema-sul-principio-attivo-valsartan-19112018
- https://www.repubblica.it/salute/medicina-e-ricerca/ … /news/non_solo_ranitidina_per_l_ema_vanno_testati_tutti_i_farmaci_per_impurita_cancerogene-237010173/
- https://www.ema.europa.eu/en/documents/scientific-discussion/prevenar-epar-scientific-discussion_en.pdf
- http://www.bollettinosifo.it/r.php?v=2598&a=26744&l=329640&f=allegati/02598_2016_06/fulltext/05_EspOpin_Cannizzo.pdf



